参考观研天下发布《2018年中国化学药品制剂行业分析报告-市场运营态势与发展趋势研究》
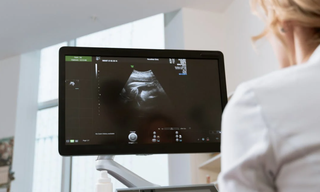
不能提供实验室中pH计、电热鼓风干燥箱等仪器设备的使用记录、消毒剂管理不规范……10日,国家药品监督管理局(简称药监局)在网站通报对山东银河生物科技有限公司飞行检查结果,发现该公司在质量管理、厂房与设施方面存在严重问题,责成企业限期整改。飞行检查是什么,包含哪些内容,对确保公众用药安全有着怎样的意义?就这些问题,记者12日随药监局对国家食品药品监督管理总局食品药品审核查验中心(简称核查中心)进行了现场调研。正是他们,承担着我国特殊食品、药品、医疗器械、化妆品等现场检查工作。
从国家食品药品监督管理总局2018年1月9日起发布的飞检通告,涉及58家生产、经营企业,21个省、直辖市及自治区,从企业所在地区的分布上来看,华东地区以18家企业的数量成为飞检最密集的地区(见图一)
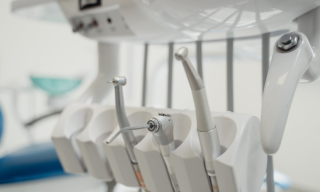
在2018年上半年的58家被飞检企业中,有28家经营企业和30家生产企业。针对不同类型产品的生产企业,药监部门将生产企业按产品划分为5大类型,分别为无菌、植入性、体外诊断试剂(以下简称IVD)、义齿类和其他。从目前飞检到的企业数量来看,植入类产品生产企业数量最多,涉及9家(见图三)。
2018年上半年医疗器械生产企业的飞检主要集中在5、6月份,涉及北京、湖北、重庆、江苏、四川、广东、海南、浙江、湖南、山东、甘肃、江西、天津、上海、河北等30家械企,植入器械生产企业7家,义齿生产企业6家,无菌器械生产企业4家,体外诊断试剂生产企业2家。其中湖北的2家企业,重庆、海南、湖南、甘肃各1家企业被责令停产整改,其余24家企业按照要求限期整改。这30家企业中,有7家企业因场地搬迁、装修、注销生产许可证等原因已经停止生产,剩余23家生产企业共查出缺陷项247项,其中严重缺陷23项,一般缺陷224项。虽然查出的严重缺陷项不多,但只要查出严重缺陷存在,均被责令停产整改!可以看出对生产企业,尤其是严重缺陷的处罚是非常严格的。

【版权提示】观研报告网倡导尊重与保护知识产权。未经许可,任何人不得复制、转载、或以其他方式使用本网站的内容。如发现本站文章存在版权问题,烦请提供版权疑问、身份证明、版权证明、联系方式等发邮件至kf@chinabaogao.com,我们将及时沟通与处理。